2023年初中化学酸碱盐知识:酸及酸的通性
2023-06-13 14:26:44佚名
 点击免费领取中考核心考点资料!
点击免费领取中考核心考点资料!
酸及酸的通性
酸的定义,电离时生成的阳离子全部都是H+。酸是由氢离子和酸根离子构成。
1.浓盐酸、浓硫酸的物理性质、特性、用途
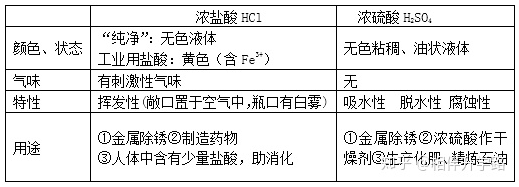
2.酸的通性:盐 酸 HCl 硫 酸 H2SO4
酸使紫色石蕊试液变红,使无色酚酞试液不变色。
金属+酸→盐+氢气
Zn+2HCl=ZnCl2+H2↑
Zn+ H2SO4 =ZnSO4+H2↑
碱性氧化物+酸→盐+水
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
碱+酸→盐+水
NaOH+HCl=NaCl+ H2O
Cu(OH)2+H2SO4= CuSO4+2H2O
盐+酸→另一种盐+另一种酸
AgNO3+HCl=AgCl↓+HNO3
BaCl2+H2SO4=BaSO4↓ +2HCl
注意:(1)在‘金属+酸→盐+氢气’中,酸通常指的是稀硫酸和稀盐酸,不能是浓硫酸或硝酸。
因为浓硫酸或硝酸都有强氧化性,与金属反应时不能生成氢气而生成了水。
(2)通过金属跟酸的反应情况导出金属活动顺序表:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
金属活动性由强逐渐减弱金属活动性顺序中,金属位置越靠前,活动性越强,反应越剧烈,所需时间越短。
(3)浓硫酸具有吸水性,通常用它作为干燥剂。
硫酸还具有脱水性,它对皮肤或衣服有很强的腐蚀性。
稀释浓硫酸时一定要把浓硫酸沿着器壁慢慢地注入水里,并不断搅动,切不可把水倒进浓硫酸里,如果把水注入浓硫酸里,水的密度较小,会浮在硫酸上面,溶解时放出的热会使水立刻沸腾,使硫酸液向四处飞溅,容易发生事故。
编辑推荐:
最新中考资讯、中考政策、考前准备、中考预测、录取分数线等
中考时间线的全部重要节点
尽在"中考网"微信公众号




