2023年初中空气中氧气含量的测定知识点总结及拓展实验
 点击免费领取中考核心考点资料!
点击免费领取中考核心考点资料!
一、拉瓦锡测定氧气的含量
1.测定原理
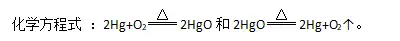
2.实验装置
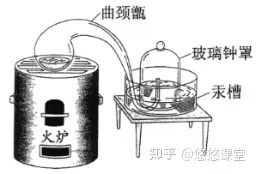
汞槽中汞的作用是,作反应物,起液封作用,
二、吸水法测定氧气的含量
1.测定原理
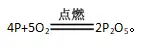
利用燃烧法测定空气中氧气的含量的原理是利用红磷燃烧消耗密闭容器内空气中的氧气,使密闭容器内压强减小,在大气压的作用下,进入容器内水的体积即为减少的氧气的体积。反应的化学方程式
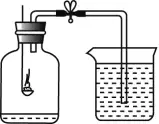
2.实验装置
(1)仪器:集气瓶、燃烧匙、导管、烧杯、橡胶管、弹簧夹。
(2)药品:红磷、水。
3.实验步骤
(1)先在集气瓶内加入少量水,并做上记号。
(2)连接装置。
(3)检查装置的气密性。
(4)用弹簧夹夹紧橡胶管。
(5)点燃红磷,迅速伸入集气瓶内。
(6)燃烧结束冷却至室温后,打开弹簧夹。
4.实验现象
① 红磷燃烧,产生大量白烟(五氧化二磷小颗粒);② 放热;③ 冷却后打开弹簧夹,水沿着导管进入集气瓶中,进入集气瓶内水的体积约占集气瓶空气总体积的1/5。
5.实验成功的关键
(1)红磷要过量。
(2)装置必须密封。
(3)导管内先注满水。
(4)冷却到室温后,打开弹簧夹。
6.实验分析与结论
红磷燃烧生成五氧化二磷固体,五氧化二磷极易溶于水,不占有体积。红磷燃烧消耗了集气瓶内的氧气,冷却后,大气压把烧杯内的水压进集气瓶,压进的水的体积约是集气瓶内消耗的氧气的体积,由此证明空气中氧气约占空气总体积的 1/5。
注意:通过此实验也能得出氮气不燃烧、不支持燃烧及不易溶于水的性质。
7.实验注意事项
1. 红磷必须过量。如果红磷的量不足,集气瓶内的氧气没有被完全消耗,测量结果会偏小。
2. 装置气密性要好。如果装置的气密性不好,集气瓶外的空气进入集气瓶,测量结果会偏小。
3. 导管中要注满水。否则当红磷燃烧并冷却后,进入的水会有一部分残留在试管中,导致测量结果偏小。
4. 冷却后再打开弹簧夹,否则测量结果偏小。
5. 如果弹簧夹未夹紧,或者塞塞子的动作太慢,测量结果会偏大。
6. 在集气瓶底加水的目的:吸收有毒的五氧化二磷。
7. 不要用木炭或硫代替红磷!原因:木炭和硫燃烧尽管消耗气体,但是产生了新的气体,气体体积不变,容器内压强几乎不变,水面不会有变化。而细铁丝在空气中难以燃烧,氧气的体积几乎不会变化,因此密闭容器内水面不上升。
8. 如果预先在集气瓶内放入氢氧化钠溶液,就可以用木炭或硫代替红磷进行实验。
9. 不要用镁代替红磷!原因:镁在空气中燃烧时能与氮气和二氧化碳发生反应,这样不仅消耗氧气,还消耗了氮气和二氧化碳,使测量结果偏大。
三、注射器法测量氧气的含量(拓展延伸)
1.原理
在加热的条件下,铜能跟空气中的氧气反应,消耗了密闭容器中的氧气,没有其他气体产生,减少的气体体积即为空气中氧气的体积。反应的化学方程式:
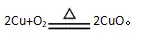
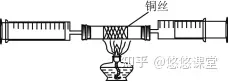
2.实验装置(如图所示)
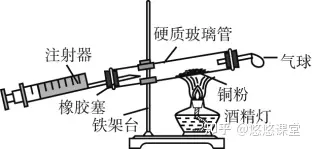
3.实验仪器
硬质玻璃管(相同规格
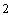
支)、橡皮塞(带玻璃导管及不带玻璃导管各
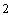
个)、量筒、酒精灯、铁架台(带
铁夹)、注射器、气球、铜粉。
4.实验步骤
(1)将一支硬质玻璃管注满水(两端用橡皮塞封住),然后打开上端橡皮塞,将水倒入量筒中,记录体积。
(2)在另一支干燥的硬质玻璃管中装入铜粉,两端塞上带玻璃导管的橡皮塞,其中一端用气球密封。移动注射器活塞,在注射器中留下一定体积的气体,记录体积后与硬质玻璃管另一端密封连接。根据酒精灯的高度,将玻璃管固定在铁架台上。
(3)用酒精灯在铜粉部位加热,加热时不断推拉注射器。
(4)停止加热后,待玻璃管冷却至室温,将气球内的气体全部挤出。待注射器活塞稳定后,记录注射器中气体的体积。
5.实验现象
铜粉加热后变成黑色,冷却至室温后,密闭装置内气体的体积减少了1/5。
6.实验结论
空气中氧气约占空气体积的1/5。
7.注意事项
(1)铜粉要足量。
(2)装置不能漏气。
(3)加热温度要高一些,时间要长一些,目的是保证铜粉和氧气充分反应。
(4)加热时为保证氧气充分反应,要不断推拉注射器活塞。
(5)冷却至室温后,读取注射器内剩余气体体积。
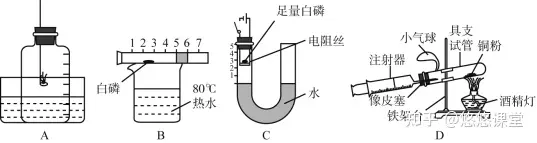
拓展:测定空气中氧气含量的装置还有如图所示A、B、C、D、E。